 |
本报记者 朱萍 北京报道
出于临床试验资源少、价格水涨船高的原因,药企纷纷放弃大量新药审批。
近日,多家药企负责人向21世纪经济报道表示,将只选取部分有竞争力的报批药品进行BE等效试验。其中一家上市药企董事长称,公司目前有3个药品在CFDA待审,但由于成本较 高,尤其是BE(体内生物等效性评价,评价仿制药质量试验)试验费高昂,所以仅选一个通过性较高的产品进行报批。
“按照企业研发制剂的规律,一个药品极有可能需要多次BE试验才能通过。若企业现有批号药品全部完成BE试验,将支付巨额资金。”上述董事长向21世纪经济报道表示。据介绍,目前国内单个品种药物的一致性评价市场报价已达300万-600万,整个行业或将面临900亿的巨额开支。
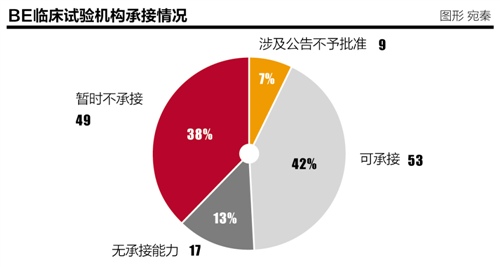
CFDA药品审核中心药物临床试验登记与信息公示平台显示,截至至2016年5月12日,平台登记的试验总数为5179项。国泰君安指出,由于临床机构在链条中属于稀缺资源,在本次一致性评价中处于相对强势地位,议价能力更高。“若所有品种都选择BE试验,受制于临床试验资源、受试者、样品分析和存储等因素的约束,按时完成评价存在较大压力。”
BE试验资源严重短缺
2016年3月5日,国务院办公厅印发《关于开展仿制药质量和疗效一致性评价的意见》,要求2007年10月1日前批准上市的化学药品仿制药、口服固体制剂,应在2018年底前完成一致性评价。
而根据2015年11月发布的230号文和231号文,对于仿制药原则上企业应采用BE评价。
截至2016年5月12日,平台登记的试验总数为5179,年度登记临床试验总数从2014年起逐年下降,即使2015年12月BE制放开,也没能挽回当年下降的趋势。
全国人大代表、辰欣药业董事长杜振新在在今年全国“两会”提交的议案中也提到这一现象,并指出BE试验资源严重不足成为近几年制约国内仿制药开发和一致性评价的瓶颈。
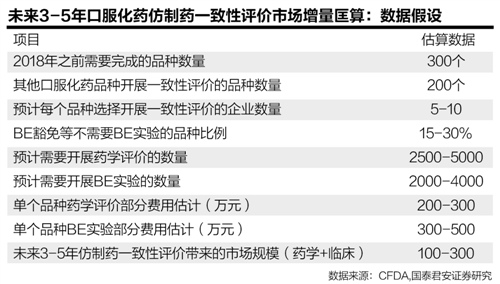
“本次仿制药一致性评价将带来整体CRO(药物研发外包)行业的扩容,根据我们从评价品种数量、可豁免数量、临床试验费用等角度匡算,目前化学药口服固体制剂的批文大约6万个,其中涉及约3000个品种数量,但考虑到推进节奏和企业现实选择,未来3-5年内开展一致性评价的品种数大约只有500个。”国泰君安指出。
在国泰君安看来,本次一致性评价涉及到的潜在品种数量规模巨大,如果所有品种都选择BE试验,受制于临床试验基地资源、受试者、样品分析和存储等因素的约束,按时完成评价存在较大压力,尤其是临床机构数量上明显不足。
海安必生制药CEO雷继峰介绍,目前有资质从事BE研究的GCP机构数量仅为100多家,加之CFDA严格核查临床试验数据造成的成本大幅上升和风险增大,GCP承接BE试验研究的积极性下降,现有BE资源无法完成大幅超量的研究任务。
据了解,自CFDA在2015年11月11日曝光临床数据造假后,严查临床试验数据已成为常态,而且对试验造假者的惩罚力度也在加大,所以尽管现在BE价格明显提升,但临床试验基地、CRO等会因BE项目风险太高,而不愿轻易启动新项目。今后临床试验基地和CRO将更愿意做质量有保障且回报率高的项目。
一位中药上市药企董事长向21世纪经济报道表示,去年公司有一个审批项目被撤下,并非自身数据有问题,而是BE机构在CFDA允许自查主动撤回时,要求其撤下的,因为该机构的其他项目存在数据问题。“现在这家机构接项目很谨慎了。”
纷纷放弃部分新药报批
事实上,很多企业掌握的药品文号数以百计,由于评价时间和地区不同,每条批文完成评价的花费在十几万到几十万不等。
亚宝药业集团股份有限公司董事长任武贤向21世纪经济报道表示,此前做一致性评价的成本是50万-60万元,但国家要求做一致性评价后,价格翻了好几番,“现在300万元是人情价,将来的价格将在500万元以上。”
另一位不愿具名的药企董事长则表示,上述费用估算过于乐观。仿制药一致性评价的成本在800万元以上。“有的仿制药按照原研药做对标,再评价成本较低,几十万元就够了;但更多仿制药是三仿、四仿做对标,再评价相当于重新研发,原来很多数据都是错的,这个成本很容易就过千万元了。”
所谓“对标”,是指仿制药应参照原研药的质量和疗效标准,成为与原研药具有相同活性成分、剂型、给药途径和治疗作用的药品,在临床上与原研药可相互替代。
其中,每次评价都需要做BE试验,而且按照企业研发制剂的规律,一个药品极有可能需要开展多次BE试验。“很多药企在协和医院完成一个BE试验,需要400万元的费用,一位上市药企董事长称。”
申万宏源分析,中国约有11万个化学药批文,按每个500万元的一致性评价费用测算,假设十年完成全部再评价工作,全行业面临5500亿元的资金投入,平均每年投入约550亿元,占中国医药行业收入约5%,而当前行业平均研发投入仅占收入约2%。
与此同时,北京鼎臣医药咨询负责人史立臣指出,目前每个药品一致性评价申请时间需要1-2年,想要在2018年底完成所有文号的申请很困难。按现有文号的数量计算,全部过一遍需要花费十多年。在临床研究机构数量有限的情况下,一致性评价工作还会大量挤压掉创新药临床试验的机会。
“企业需要做出抉择,或保留大品种药物,或力保独家品种,肯定需要选择有竞争优势、技术难度的药物进行评价申请,而且会主动选择放弃现有文号的申请,选择投入新的研发领域。”史立臣表示。
据了解,多家药企已经放弃竞争性不强的新药审批。康芝药业一位负责人向21世纪经济报道表示,虽然现在儿童用药前景广阔,我们也有很多在研产品,但考虑成本和市场竞争,也将放弃部分新药审批。
而上药集团因涉及品种众多,将销售规模、盈利能力、原料配套基础等要素纳入综合评价指标,将优先开展重点品种和药品招标中有优势的低价药、妇科、儿科用药领域品种的一致性评价。(编辑 陆宇)
 |
作者:朱萍










 动物系恋人啊 | 钟欣潼体验爱情哲学
动物系恋人啊 | 钟欣潼体验爱情哲学 南方有乔木 | “科创CP”渐入佳境
南方有乔木 | “科创CP”渐入佳境 魔都风云 | 周冬雨任达华演父女
魔都风云 | 周冬雨任达华演父女







我来说两句排行榜